2025年8月25日,广州医科大学附属第一医院何建行教授团队在《自然-医学》期刊发表研究成果,宣布完成全球首例基因编辑猪肺移植至脑死亡人体的临床前试验。该案例将六基因编辑巴马香猪左肺植入39岁脑死亡男性受体,成功维持肺功能9天,期间未发生超急性排斥反应或病原体感染,标志着异种肺移植领域取得关键性进展。
01
基因编辑策略
供体猪采用CRISPR技术进行六处关键基因改造:敲除α-1,3-半乳糖基转移酶(GGTA1)、β-1,4-N-乙酰半乳糖胺转移酶(CMAH)等免疫原性基因,同时过表达人源CD46、CD55等补体调节蛋白。这种"减法加法"结合的编辑策略,有效降低了异种免疫排斥风险。
手术实施与监测
研究团队模拟临床单肺移植场景,通过微创导管技术将基因编辑猪肺植入受体。术后监测数据显示:移植肺通气功能正常,血氧饱和度维持在95%以上,胸部CT显示肺组织结构清晰,无渗出性病变。值得注意的是,术后24小时出现轻度肺水肿,经调整免疫抑制方案后逐步缓解。
免疫抑制方案
采用多靶点联合用药策略,包括抗胸腺细胞球蛋白、巴利昔单抗、利妥昔单抗等,术后根据免疫状态动态调整。西班牙国家移植组织主任比阿特丽斯·多明格斯-希尔评价:"该方案为解决异种移植免疫调控提供了新范式。"
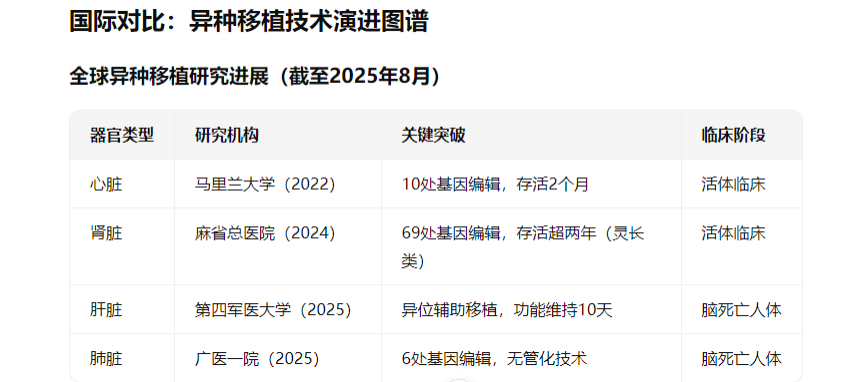
相较于美国团队的多基因编辑策略(如eGenesis公司猪的69处修改),中国方案聚焦关键免疫靶点,在保证有效性的同时降低了技术复杂度。西班牙专家特别指出:"肺移植因生理脆弱性(高血流、空气暴露)面临更大挑战,中国成果是该领域的里程碑。"
02伦理与法规:创新与规范的平衡
研究方案经广州医科大学附属第一医院伦理委员会三次全体会议审议,重点评估脑死亡判定标准、受体选择依据及知情同意流程。
受体为重型颅脑损伤患者,经六位神经科专家独立评估,确认符合中国脑死亡判定标准(2018版),包括深昏迷、脑干反射消失、无自主呼吸三项核心指标。
家属签署知情同意书时,研究团队采用可视化工具展示异种移植潜在风险与科学价值,确保决策过程透明。
何建行团队规划三阶段发展路径:
技术优化期(2025-2027):完成10例以上脑死亡受体移植,将供体肺功能维持时间延长至30天,同步开展人源化巨噬细胞移植研究。
活体试验期(2028-2030):选择终末期肺纤维化患者(预计全球年需求量超10万例),采用"桥接治疗"方案,争取5年生存率达70%。
商业化阶段(2031+):建立区域化异种移植中心,配套开发AI配型系统与个性化免疫监控平台,目标将治疗成本控制在传统肺移植的60%以下。
这一突破不仅标志着中国在生物医学工程领域跻身国际第一梯队,更可能重塑全球器官移植格局。正如《自然-医学》审稿专家评价:"该研究将异种移植从概念验证推向临床前阶段,为数百万等待器官的患者点燃了希望之光。"随着基因编辑技术与免疫调控策略的持续突破,异种器官移植有望在十年内成为常规治疗手段,彻底改写终末期器官衰竭患者的命运。
特别声明:智慧医疗网转载其他网站内容,出于传递更多信息而非盈利之目的,同时并不代表赞成其观点或证实其描述,内容仅供参考。版权归原作者所有,若有侵权,请联系我们删除。
凡来源注明智慧医疗网的内容为智慧医疗网原创,转载需获授权。